سریم «برادر بزرگ» بلامنازع در خانواده بزرگ عناصر خاکی کمیاب است. اولاً، فراوانی کل عناصر خاکی کمیاب در پوسته زمین 238ppm است که سریم با 68ppm، 28٪ از کل ترکیب عناصر خاکی کمیاب را تشکیل میدهد و رتبه اول را دارد. ثانیاً، سریم دومین عنصر خاکی کمیاب است که نه سال پس از کشف ایتریم (1794) کشف شد. کاربرد آن بسیار گسترده است و «سریم» غیرقابل توقف است.
کشف عنصر سریم

کارل آور فون ولزباخ
سریم در سال ۱۸۰۳ توسط کلوپرز آلمانی، شیمیدان سوئدی، یاکوب برزلیوس و کانیشناس سوئدی، ویلهلم هیزینگر، کشف و نامگذاری شد. به یاد سرس، سیارکی که در سال ۱۸۰۱ کشف شد، این عنصر سریا و سنگ معدن آن سریت نامیده میشود. در واقع، این نوع سیلیکات سریم، نمکی هیدراته است که حاوی ۶۶٪ تا ۷۰٪ سریم است، در حالی که بقیه ترکیباتی از کلسیم، آهن و ... هستند.ایتریم.
اولین کاربرد سریم در شومینه گازی بود که توسط شیمیدان اتریشی، کارل آور فون ولزباخ، اختراع شد. در سال ۱۸۸۵، او تلاش کرد تا مخلوطی از منیزیم، لانتانیم و اکسید ایتریم را تولید کند، اما این مخلوطها بدون موفقیت، نور سبز ساطع میکردند.
در سال ۱۸۹۱، او دریافت که اکسید توریم خالص نور بهتری تولید میکند، اگرچه آبی بود، و آن را با اکسید سریم(IV) مخلوط کرد تا نور سفید درخشانی تولید کند. علاوه بر این، اکسید سریم(IV) همچنین میتواند به عنوان کاتالیزوری برای احتراق اکسید توریم استفاده شود.
فلز سریم

★ سریم فلزی نرم، چکشخوار و به رنگ سفید نقرهای است که خواص فعالی دارد. در صورت قرار گرفتن در معرض هوا، اکسید شده و یک لایه اکسید زنگمانند تشکیل میدهد. در صورت گرم شدن، میسوزد و به سرعت با آب واکنش میدهد. یک نمونه سانتیمتری از فلز سریم ظرف حدود یک سال کاملاً خورده میشود. از تماس با هوا، اکسیدانهای قوی، اسیدهای قوی و هالوژنها خودداری کنید.
★ سریم عمدتاً در مونازیت و باستنازیت و همچنین در محصولات شکافت اورانیوم، توریم و پلوتونیوم وجود دارد. از آنجایی که برای محیط زیست مضر است، باید به آلودگی منابع آبی توجه ویژهای شود.
★ سریم بیست و ششمین عنصر فراوان است که ۶۸ppm پوسته زمین را تشکیل میدهد و پس از مس (۶۸ppm) در رتبه دوم قرار دارد. سریم از فلزات معمولی مانند سرب (۱۳ppm) و قلع (۲.۱ppm) فراوانتر است.
پیکربندی الکترونی سریم
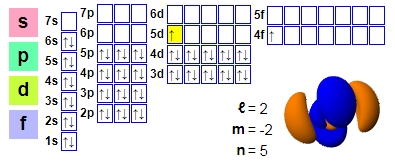
ترتیبات الکترونیکی:
۱s۲ ۲s۲ ۲p۶ ۳s۲ ۳p۶ ۴s۲ ۳d۱۰ ۴p۶ ۵s۲ ۴d۱۰ ۵p۶۶s۲ ۴f۱ ۵d۱
★ سریم بعد از لانتانیم قرار دارد و دارای الکترونهای 4f است که از سریم شروع میشوند و شرکت در واکنشهای شیمیایی را آسان میکنند. با این حال، اوربیتال 5d سریم اشغال شده است و این اثر در سریم به اندازه کافی قوی نیست.
★ اکثر لانتانیدها فقط میتوانند از سه الکترون به عنوان الکترون ظرفیت استفاده کنند، به استثنای سریم که ساختار الکترونی متغیری دارد. انرژی الکترونهای 4f تقریباً برابر با الکترونهای خارجی 5d و 6s غیرمستقر در حالت فلزی است و تنها مقدار کمی انرژی برای تغییر اشغال نسبی این سطوح انرژی الکترونیکی مورد نیاز است که منجر به ظرفیت دوگانه +3 و +4 میشود. حالت عادی +3 ظرفیت است که در آب بیهوازی +4 ظرفیت را نشان میدهد.
کاربرد سریم

★ میتواند به عنوان افزودنی آلیاژ و برای تولید نمکهای سریم و غیره استفاده شود.
★ میتواند به عنوان افزودنی شیشه برای جذب اشعه ماوراء بنفش و مادون قرمز استفاده شود و به طور گسترده در شیشه خودرو استفاده میشود.
★ میتواند به عنوان یک ماده عالی برای حفاظت از محیط زیست مورد استفاده قرار گیرد و در حال حاضر، نمایندهترین آن کاتالیزور تصفیه اگزوز خودرو است که به طور موثر از تخلیه مقدار زیادی گاز اگزوز خودرو به هوا جلوگیری میکند.
★ نورعناصر خاکی کمیابعمدتاً از سریم تشکیل شده است، زیرا به عنوان تنظیمکنندههای رشد گیاهی میتوانند کیفیت محصول را بهبود بخشند، عملکرد را افزایش دهند و مقاومت محصول در برابر تنش را افزایش دهند.
★ سولفید سریم میتواند جایگزین فلزاتی مانند سرب و کادمیوم شود که برای محیط زیست و انسان مضر هستند، در رنگدانهها، میتواند پلاستیکها را رنگ کند و همچنین میتواند در صنایع پوشش و جوهر استفاده شود.
★اکسید سریم(IV)میتواند به عنوان ترکیب صیقلدهنده، به عنوان مثال، در صیقلدهی شیمیایی-مکانیکی (CMP) استفاده شود.
★ سریم همچنین میتواند به عنوان مواد ذخیرهسازی هیدروژن، مواد ترموالکتریک، الکترودهای تنگستن سریم، خازن سرامیکی، سرامیکهای پیزوالکتریک، سایندههای کاربید سیلیکون سریم، مواد اولیه پیل سوختی، کاتالیزورهای بنزین، مواد مغناطیسی دائمی، مواد پزشکی، فولادهای آلیاژی مختلف و فلزات غیر آهنی استفاده شود.
زمان ارسال: 3 ژوئیه 2023